Desde los años 80 es conocido que las enfermedades relacionadas con la nutrición tienen un componente genético o heredable. Las nuevas tecnologías y la secuenciación completa del genoma humano en 2001 han permitido avances en el conocimiento de las interacciones gen-dieta que plantean un horizonte muy prometedor enfocado hacia la nutrición personalizada.
Es de sobra conocido que las epidemias que afectan hoy en día a las poblaciones de todo el planeta ya no se deben a enfermedades infecciosas sino a aquellas que se conocen como enfermedades no transmisibles u occidentales.
La más estudiada de todas es la obesidad. La Organización Mundial de la Salud (OMS) estima que, en 2015, el exceso ponderal afectará a más de 1500 millones de personas, lo que supone un 21% de la población mundial.
A esta patología debemos sumarle otras que constituyen lo que se conoce como síndrome metabólico: diabetes, hipertensión, hipercolesterolemia, hipertrigliceridemia, etc., conducentes a enfermedades de tipo cardiovascular y a cáncer.

Las causas que conducen a este tipo de alteraciones metabólicas han sido ampliamente estudiadas y, en su mayoría, se han asociado con la transición nutricional y con cambio de estilo de vida: aumento del consumo de alimentos ricos en grasas saturadas, carbohidratos refinados y sodio, así como al disminución de la actividad física cotidiana y las horas de descanso nocturno y unido al aumento del nivel de estrés.
Desde finales de los años 80, comenzó una corriente científica que buscó explicaciones más allá de los factores ambientales ya mencionados. Suscitados por la evidencia de que no todas las personas respondían con igual eficacia ante un mismo tratamiento dietético, los investigadores centraron su atención en la genética.
Uno de los primeros trabajos al respecto se publicó en el año 1988 en la revista American Journal of Clinical Nutrition (1) cuyo resumen comienza así: “La genética determinan diferencias en la habilidad de transportar o metabolizar determinados constituyentes dietarios (o sus metabolitos) y esto contribuye a diferente susceptibilidad a enfermedades”.
Descubriendo la genética de la obesidad
Al final de la década de los 80 y principio de los 90, fueron comunes los estudios con gemelos encaminados a conocer el grado de heredabilidad del exceso de peso. El más reseñable es el de la National Academy of Sciences con datos de 15,924 gemelos varones recogidos durante su servicio militar (2). En este trabajo concluyeron el índice de masa corporal (IMC) tiene una heredabilidad del 77%, esto quiere decir que el IMC de una persona dependería en un 77% de la genética familiar y en un 23% del ambiente.

Otros estudios, han demostrado un valor similar de heredabilidad del componente graso (74%-84%) medido a través de pliegues adiposos subcutáneos (3). Sin embargo todos estos trabajos se hicieron en una época en la que la tecnología aun no estaba desarrollada por lo que, a pesar de confirmar que el componente genético tenía una gran importancia, se desconocían los genes concretos que predisponían a obesidad.
Con la tecnología algo más avanzada comenzaron a conocerse los genes que estaban implicados en los casos de obesidad mórbida (IMC superior a 40 kg/m2). En general esta patología está determinada por una mutación en un único gen concreto por lo que se la conoce como obesidad monogénica (los genes más estudiados están relacionados con la leptina y la melanocortina). Este tipo de obesidad es patente desde la niñez y suele manifestarse con otros síntomas por lo que también se le conoce como obesidad sindrómica. El síndrome más frecuente es el de Prader-Willi y afecta a 1 de cada 25.000 personas, otros conocidos son el Bardet-Biedl, Cohen, Ayazi y el síndrome MOMO.

Sin embargo, las mutaciones de un solo gen sólo pueden explicar el 5% de la obesidad mundial. El otro 95% se corresponde con la obesidad común, la cual, está regulada por múltiples genes cuyo efecto individual sería despreciable pero, en conjunto, predisponen a la enfermedad (4). Gracias al conocimiento completo del genoma humano publicado en 2001 y a las avanzadas técnicas moleculares, hoy en día se siguen descubriendo regiones mutadas del ADN relacionadas con valores elevados de IMC o de porcentaje de grasa. Todas estas variaciones genéticas se dan a conocer mediante el “Human Obesity Gene Map” (5).
Esta predisposición genética, unida a un ambiente obesogénico (mala alimentación y baja actividad física) es lo que hace que hoy en día mueran 2,6 millones de personas al año, según cifras de la OMS.
Epigenética: el ADN modificado más alla de su secuencia
Hasta hace relativamente poco tiempo se pensaba que sólo si se daban mutaciones en la secuencia de ADN, estas modificaciones podían pasar de generación en generación. Sin embargo esto no es del todo cierto ya que se ha descubierto que existen factores ambientales que pueden activar o desactivar genes, modificando la estructura química del ADN pero sin que haya cambio en su secuencia de nucleótidos y, contra lo que se pensaba, estas modificaciones son heredables de padres a hijos y nietos. Al estudio de estos factores se le conoce como epigenética.
La modificación química más corriente es la metilación del ADN: adición de un grupo metilo en la posición 5 del anillo de pirimidina de la citosina o en el número 6 del nitrógeno del anillo de purina de la adenina (citosina y adenina son dos de las cuatro bases nitrogenadas posibles en la secuencia del ADN). Esta adición no hace que una base nitrogenada se convierta en otra, por lo que no altera la secuencia del ADN.
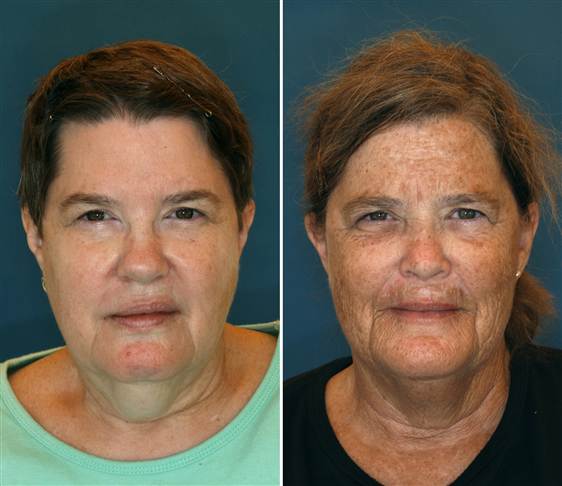
Para explicarlo con un ejemplo, un factor epigenético para el ser humano es el consumo de tabaco. Obviamente, fumar no va a cambiar nuestra secuencia de ADN pero si aumenta los radicales libres en nuestro organismo los cuales pueden metilarlo. Para demostrarlo os dejamos el caso de las gemelas Jeanne (izquierda) no fumadora y Sarah (derecha) si fumadora, sacado de una noticia de la cadena NCB estadounidense en 2009 (http://www.nbcnews.com/id/33385839/#.UnwxZ_k9qSo).
En la foto puede verse claramente los efectos del tabaco sobre la piel. Os recomendamos que visitéis el enlace de esta noticia y repaséis el resto de casos de gemelos genéticamente idénticos pero diferenciados por el ambiente .
Genómica nutricional: somos lo que comemos

Existen diversos factores epigenéticos además del tabaco, como pueden ser pocas horas de sueño (ritmos circadianos alterados), el estrés, etc. Pero el más importante de estos factores relacionado con la salud de los humanos es su alimentación y de su estudio se encarga la genómica nutricional.
El investigador español y presidente de honor de la revista de la SEDCA, el Dr. José María Ordovás, es considerado el padre de esta disciplina. Según sacamos de uno de sus artículos: “la genómica nutricional estudia las interacciones funcionales de los alimentos y sus componentes con el genoma a nivel molecular, celular y sistémico, con el objetivo de prevenir o tratar enfermedades a través de la dieta” (6).
Esta interacción entre genes y dieta es de doble sentido y, en función de ello podemos encontrar dos tipos de ciencia:
- Nutrigenómica(dieta -> gen): Estudia el efecto que la alimentación ejerce en nuestra salud al modificar la expresión de nuestros genes. Hablando menos científicamente, pero de forma más esclarecedora, podríamos resumirla en “lo que como modifica lo que soy”.
- Nutrigenética (gen -> dieta): Estudia las variantes genéticas (diferencias en la secuencia de ADN) asociadas con predisposición a enfermedades por respuesta diferencial ante una misma alimentación. Resumiendo: “lo que soy determina cómo me influye lo que como”.
La genómica nutricional, por tanto, tiene como finalidad acumular conocimiento que permita el desarrollo de la nutrición o medicina personalizada: en función de nuestro genotipo, elaborar dietas o precisas la dosis adecuada de un medicamento que nos permita evitar o curar las enfermedades asociadas con el síndrome metabólico. Hasta el momento, la nutrición personalizada es una utopía ya que aún queda mucho por estudiar, sobre todo tratándose de una disciplina tan nueva.
Para finalizar, queremos destacar que el pasado mes de Septiembre se publicó el primer estudio epigenético a gran escala (epigenome wide association study, EWAS) (7) que pretendía relacionar este tipo de modificaciones del ADN con parámetros séricos sintomáticos de alteraciones metabólicas (glucosa elevada, colesterol elevado, etc). En él, los autores afirma categóricamente que la metilación del ADN juega un importante papel regulador en el metabolismo humano.
Referencias:
1.- Holtzman NA. Genetic variation in nutritional requirements and susceptibility to disease: policy implications. Am J Clin Nutr, 1988; 48: 1510-1516. http://ajcn.nutrition.org/content/48/6/1510.long
2.- Stunkard et al. A twin study of human obesity. J Am Med Assco, 1986; 256 (1): 51.
3.- Bodurtha et al. Genetic analysis of anthropometric measures in 11 year old twins: the Medical College of Virginia Twin Study. Pediatr Res, 1990; 28:1.
4.- Marrodán et al. La obesidad poligénica, aportación de los SNP (Single Nucleotide Polimorphism). En: Avances en Alimentación, Nutrición y Dietética (Ed. Fundación Alimentación Saludable). Madrid, 2012. pp. 173-183.
5.- Rakinen et al. The human obesity gene map: the 2005 update. Obesity, 2006; 14: 529-644.
6.- Ordovás y Carmena. Nutrigenómica y Nutrigenética. En: Monografías Humaitas nº9. Fundación Medicina y Humanidades Médicas. Barcelona, 2006. pp. 21-44. http://www.fundacionmhm.org/pdf/Mono9/Articulos/articulo1.pdf
7.- Petersen et al. Epigenetics meets metabolomics: an epigenome-wide association study with blood serum metabolic traits. Hum Mol Genet, Sept. 2013.
Noticia elaborada por Noemí López-Ejeda (Asociada SEDCA) @LopezEjedaN en Twitter
