Además de evitar su contaminación por los cereales más tóxicos, hay que controlar que el contenido en proteínas inmunogénicas presentes en la avena sea indetectable por las técnicas analíticas de última generación. Los celíacos deberían tener, en cualquier caso, cierta cautela y precaución ante el consumo de avena.
Los celíacos necesitan seguir una dieta sin gluten de por vida, lo cual supone eliminar de su alimentación el trigo, la cebada, el centeno y los alimentos derivados. Existe un cuarto cereal que ha suscitado controversias entre la comunidad celíaca y médica: la avena. Hay estudios clínicos que demuestran su seguridad y, en contraste, otros que identifican un considerable número de celíacos que son sensibles a este cereal.
Todos los cereales tienen en su composición dos tipos de proteínas del gluten diferentes, que se llaman prolaminas y glutelinas. Son las primeras las que producen mayor reacción inmunológica en los celíacos. Así, mientras que la cantidad de prolaminas del trigo es del 69%, la proteína equivalente en la avena, la avenina, es del 12 al 16% del total de sus proteínas.
Lundin y col.1 estudiaron 19 pacientes celíacos que consumieron 50 g de avena al día durante 12 semanas, de los cuales uno fue sensible a la avena. Asimismo, otros investigadores también observaron in vivo la reactividad de la avenina frente a las células T.2,3,4 Los datos obtenidos sugieren que muy probablemente no todos los pacientes celíacos tengan la misma sensibilidad a la avena, sin embargo no controlaron el origen de la avena usada.

Algunos autores han lanzado la opinión equivocada de que la pureza de la avena es suficiente para garantizar su seguridad, ya que encontraron algunas partidas de avena contaminadas con cebada y/o trigo. Sin embargo, diversos estudios de investigación con diferentes variedades de avena comerciales han demostrado que la toxicidad de este cereal varía dependiendo del cultivar o variedad empleada. 5,6,7 Para estos estudios, los granos de avena se examinaron cuidadosamente para verificar su pureza. La toxicidad de cada variedad de avena se evaluó mediante métodos basados en los anticuerpos G12 y A1 que tienen capacidad para determinar los GIP (Gluten Immunogenic Peptides) que son los responsables de la toxicidad del gluten en los pacientes celíacos.8 Las variedades estudiadas se clasificaron en tres grupos en función de su reactividad con el anticuerpo (alta reactividad, intermedia reactividad y sin reacción detectable). Así mismo, su toxicidad fue estudiada mediante linfocitos T de pacientes celíacos, demostrándose que la reactividad de los anticuerpos G12 y A1 frente a las avenas se correlacionaba con los estudios de células inmunológicas.
Otro estudio reciente de dos centros estadounidenses, ha confirmado la presencia de péptidos reconocidos por R5 en avenas puras, otro anticuerpo menos específico para la determinación de gluten tóxico pero que es ampliamente usado en laboratorios de análisis, confirmandose que algunas variedades de avenas pueden mostrar niveles de reactividad por encima del valor permitido en las legislaciones.9
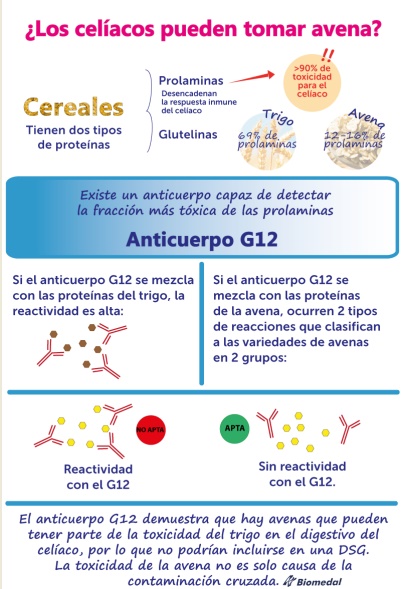
La existencia o no de avenas con esas proteínas reactivas inmunológicamente, determinan, por tanto, cómo es de tolerable cada variedad y explica por qué existían discrepancias en los estudios clínicos anteriores que no consideraron el cultivar de avena suministrado. En cualquier caso, las avenas más reactivas eran cientos de veces menos reactivas que el trigo, con lo que se necesita una ingesta mucho mayor y continua de dichas avenas reactivas para proporcionar la misma toxicidad a un celíaco que el trigo, cebada y centeno.
El descubrimiento de los grados de toxicidad potencial de la avena, abre una nueva oportunidad hacia el desarrollo de cultivares más seguros a través de la selección de avenas con menor contenido en gluten potencialmente tóxico.10
En términos prácticos y como conclusión de los estudios recientes, cualquier muestra de avena que no muestre reactividad con los métodos de última generación A1 o G12, podría definirse como segura para la gran mayoría de los celíacos ya que descartaría la presencia de péptidos tóxicos tanto de origen por contaminación como propios de la avena.
Ángel cebolla, CEO de Biomedal
Elena Moreno Portillo, bióloga y comunicadora científica
Referencias bibliográficas:
1. Lundin KE, Nilsen EM, Scott HG, y col. “Oats induced villous atrophy in coeliac disease.” Gut 2003; 52: 1649-1652.
2. Hardy MY, Tye-Din JA, Stewart JA, Schmitz F, Dudek NL, Hanchapola I, Purcell AW, Anderson RP. “Ingestion of oats and barley in patients with celiac disease mobilizes cross-reactive T cells activated by avenin peptides and immuno-dominant hordein peptides. J Autoimmun.” 2015 Jan;56:56-65.
3. Arentz-Hansen H. et al. “The Molecular Basis for Oat Intolerance in Patients with Celiac Disease.” Ed. Marco Londei. PLoS Medicine, 2004 Oct.; 1(1): e1.
4. Silano M, Pozo EP, Uberti F, Manferdelli S, Del Pinto T, Felli C, Budelli A, Vincentini O, Restani P. “Diversity of oat varieties in eliciting the early inflammatory events in celiac disease.” Eur J Nutr 2014 Aug;53(5):1177-86.
5. Comino I, Real A, de Lorenzo L, et al. “Diversity in oat potential immunogenicity: basis for the selection of oat varieties with no toxicity in coeliac disease.” Gut 2011;60:915-922.
6. Real y col. “Molecular and immunological characterization of gluten proteins isolated from oat cultivars that differ in toxicity for celiac disease”. PlosOne, 2012 Dec;7(12):e48365.
7. Comino et al. “Identification and Molecular Characterization of Oat Peptides Implicated on Coeliac Immune Response.” Food & Nutrition Research, 2016 Feb; 10.3402/fnr.v60.30324.
8. Morón B., Cebolla A., Manyani H., Alvarez-Maqueda M., Megías M., Thomas M del C., López MC., Sousa C. “Sensitive detection of cereal fractions that are toxic to celiac disease patients by using monoclonal antibodies to a main immunogenic wheat peptide.” Food Nutr Res. (2008) Feb; 87(2):405-14.
9. Benoit L, Masiri J, Del Blanco IA, Meshgi M, Gendel SM, Samadpour M. “Assessment of avenins from different oat varieties using R5-based sandwich ELISA.” J Agric Food Chem, 2017 Jan. doi: 10.1021/acs.jafc.6b05105.
10. Giménez MJ, Real A, García-Molina MD, Sousa C, Barro F. “Characterization of celiac disease related oat proteins: bases for the development of high quality oat varieties suitable for celiac patients.” Sci Rep. 2017 Feb 17;7:42588.
